科學家們發現了mRNA被輸送到細胞的秘密
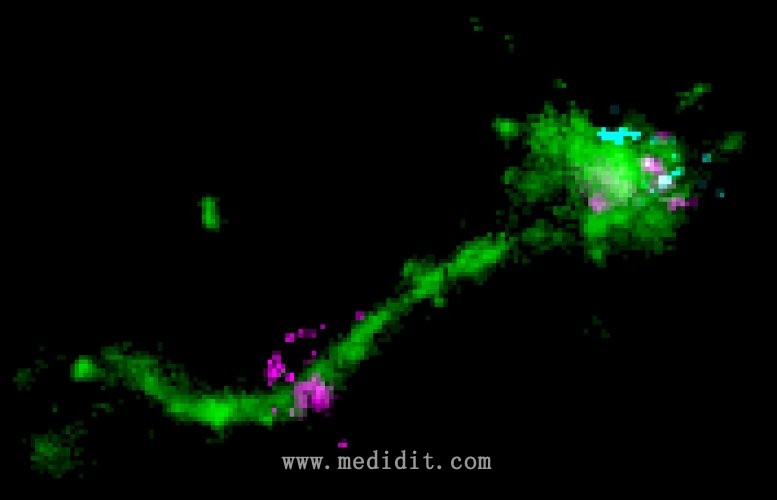
LNP 位于長的內體小管(綠色)上,與垂直分散的 mRNA 信號(青色)一起,可能代表 mRNA(紫色)逃逸的一個實例。來源:Marino Zerial / MPI-CBG
研究人員已經發現了 mRNA 在何處以及如何到達細胞以修改或傳遞遺傳信息,這是開發新療法的關鍵過程。
發現:對可能的生命起源的新見解:研究人員首次創造出可復制的 RNA 分子
DNA(脫氧核糖核酸)包含生命發育和維持所需的遺傳信息。該信息由信使核糖核酸 (mRNA) 傳遞以制造蛋白質。基于 mRNA 的療法有可能解決各種疾病的未滿足需求,包括癌癥和心血管疾病。mRNA 可以被傳遞到細胞中以觸發靶蛋白的產生、降解或修飾,這是其他方法無法做到的。
這種方式的一個關鍵挑戰是能夠將 mRNA 遞送到細胞內,以便將其翻譯成蛋白質。mRNA 可以被裝入脂質納米顆粒 (LNP) 中——脂肪的小氣泡——保護 mRNA 并將其穿梭到細胞中。然而,這個過程并不簡單,因為 mRNA 必須通過膜才能到達其在細胞內部的作用位點,即細胞質。
MPI-CBG 主任 Marino Zerial 團隊的研究人員是用高分辨率顯微鏡觀察細胞中分子(例如 mRNA)進入細胞途徑的專家。他們與來自阿斯利康(AstraZeneca)的科學家合作,他們為研究人員提供了脂質納米顆粒原型,他們開發了這些原型用于追蹤細胞內 mRNA 的治療方法。該研究發表在《細胞生物學雜志》上。
“要交付,mRNA 必須經過漫長的旅程。封閉在脂肪 LNP 氣泡中,它需要首先進入細胞,”Marino Zerial 解釋說。“LNP 到達細胞表面并與受體結合。然后它們被吸收到稱為內體的專門的膜封閉隔室中。此時,mRNA 在細胞內,但被兩個屏障包圍,脂肪泡和內體壁或更準確地說是膜。mRNA 面臨的挑戰是逃離這兩個障礙,到達細胞質,在那里它作為模板來制造蛋白質。我們知道只有一小部分RNA分子能夠逃逸到細胞質中。”
內化的貨物分子,如 LNP,首先被運輸到“早期”內體。這些是物流中心,將貨物分子分配到細胞中的各個目的地。它們要么將分子循環到細胞表面,要么在晚期內體和溶酶體中降解它們。到目前為止,人們認為 mRNA 是利用它們的酸性成分從晚期內體中逃逸出來的。
“通過單分子顯微鏡技術,”該研究的第一作者 Prasath Paramasivam 解釋說,“我們可以首次可視化細胞內體中 LNP 中的 mRNA。我們還捕捉到了 mRNA 的實際逃逸,這種逃逸發生在循環內體的小管中,這些小管只是弱酸性。我們的結果表明,將 LNP-mRNA 發送到晚期內體會適得其反,只會增加細胞毒性,”Zerial 說。這些發現有助于更詳細地了解 mRNA 從內體逃逸的機制。
Marino Zerial 總結道:“由于內體逃逸效率低,mRNA 的 LNP 遞送系統需要高劑量。了解 mRNA 的去向以及它如何逃離內體使我們能夠開發更好的載體,以更低的劑量更有效地遞送。我們可以改進 mRNA 傳遞系統,使其可用于治療應用,例如癌癥治療。”
參考文獻:
Prasath Paramasivam、Christian Franke、Martin St?ter、Andreas H?ijer、Stefano Bartesaghi、Alan Sabirsh、Lennart Lindfors、Marianna Yanez Arteta、Anders Dahlén、Annette Bak、Shalini Andersson、Yannis Kalaidzidis、Marc Bickle 和 Marino Zerial,2021 年 12 月 9 日,《細胞生物學雜志》。
DOI: 10.1083/jcb.202110137
